【文献分享】成人坏死性筋膜炎诊治专家共识(2025版)
坏死性筋膜炎(necrotizing fasciitis,NF)是一种由多种细菌混合感染引起的化脓性软组织感染,累及皮下和皮下软组织的感染性疾病,起病急,进展迅速,严重情况下可引起多脏器功能衰竭、坏疽、脓毒性休克及意识丧失等危及患者生命的并发症。
临床问题1:NF的概述
推荐意见1(强推荐)
NF是一种罕见但极为严重的化脓性软组织感染性疾病。病变主要沿筋膜平面快速扩散,常累及皮下组织及浅、深筋膜,但通常不累及肌肉层。该疾病起病急骤,进展迅猛,常伴全身性感染、中毒症状,具有发病率低但致死率高的特点。免疫功能低下的患者更易发生此类感染。证据等级:高。
证据与说明:
发病机制:致病菌侵入皮下组织后,通过释放多种毒素和酶类,破坏局部组织结构和功能,引发急性进行性坏死。与此同时,活化的免疫细胞释放大量炎症因子和细胞因子,进一步加剧炎症反应和组织损伤,导致组织广泛性炎症、充血和水肿。此外,由于血管和淋巴管受损,局部血液循环和淋巴回流受阻,使得坏死组织无法被及时清除和修复。筋膜组织结构疏松,存在自然腔隙且血液供应相对较少,这些特点致使感染更易沿筋膜进行隐匿性扩散,从而加重病情。
病理学变化:
皮肤及皮下组织广泛坏死:由于淋巴通路常被迅速破坏,故淋巴管炎和淋巴结炎较为少见,但脂肪组织常出现坏死、液化或变性。
筋膜组织广泛坏死:形成潜行腔道并扩散,这是NF的重要特征之一;镜下可见筋膜中有大量中性粒细胞浸润,动静脉壁出现纤维素性坏死。
血管:皮肤和皮下的小血管网发生炎性栓塞,导致组织营养障碍和缺血性坏死。
常见病原菌:多为需氧菌和厌氧菌的混合感染所致。
革兰阳性菌:如A组β溶血性链球菌、金黄色葡萄球菌(包括耐甲氧西林金黄色葡萄球菌)等
革兰阴性菌:(如大肠埃希菌、肺炎克雷伯菌)以及厌氧菌(如产气荚膜梭菌、脆弱拟杆菌)
此外,创伤弧菌和真菌感染相对少见。
临床问题2:NF的诊断
推荐意见2(强推荐)
早期诊断是降低NF患者病死率的关键。建议综合评估患者的易感因素、病史、特征性临床表现以及手指试验结果,并联合应用NF实验室风险指标 LRINEC、SIARI、LARINF评分等工具协助NF早期风险识别和诊断。证据等级:高。
证据与说明:
NF起病隐匿且发展迅速,延误诊断是导致其高致死率的关键因素,因此早期诊断至关重要。NF的诊断主要依赖于特征性临床表现,并结合必要的辅助检查。前述各种评分系统仅作为辅助诊断工具,不宜孤立使用。
特征性临床表现:
早期:皮肤出现局部轻度红肿,随后逐渐发展为红斑、肿胀、发热和压痛。触诊时皮肤质地较柔软,且常伴有与症状不相称的剧烈疼痛。
中期:皮肤出现皲裂,伴有水疱和大疱形成,以及一定程度的皮肤坏死。
晚期:出现出血性大疱、捻发音及皮下组织坏死。渗液为恶臭性脓液,皮下脂肪和筋膜发生水肿、渗液黏稠、浑浊、发黑,最终液化坏死。小血管血栓形成及皮下浅表神经受损,受累区域可能出现麻木感,疼痛反而减轻。患者可同时出现全身症状,如发热、心动过速、脓毒症、电解质紊乱、意识障碍等,甚至发展为脓毒症休克和MOF。在已使用静脉抗菌药物的情况下,若红斑和皮肤硬化边界仍迅速扩大,提示病情仍在进展,这是疾病早期的重要警示信号。
手指实验:疑似部位麻醉后,建议切口长度2cm至深筋膜),随后伸入手指进行探查。若探查过程中无出血但存在异味分泌物、肌肉收缩性差、手指可轻易钝性分离皮下组织与筋膜层,伴有大量稀薄的“洗肉水样脓液”,试验结果为阳性,高度怀疑为NF。
评分工具:
LRINEC 评分:当LRINEC评分≥6分时,其诊断 NF的阳性预测值为92%;而<6分时,阴性预测值为96%。可辅助诊断、评估风险及预后预测,但存在局限性,低评分不能完全排除NF的可能性(表2)。
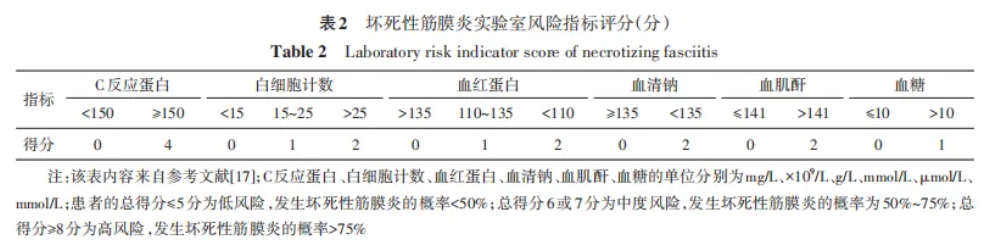
SIARI 评 分 :纳入更多关键的临床因素,提高诊断准确性,3分作为诊断阈值时,敏感度为84%,特异度为70%,有效降低漏诊率和误诊率(表3)。
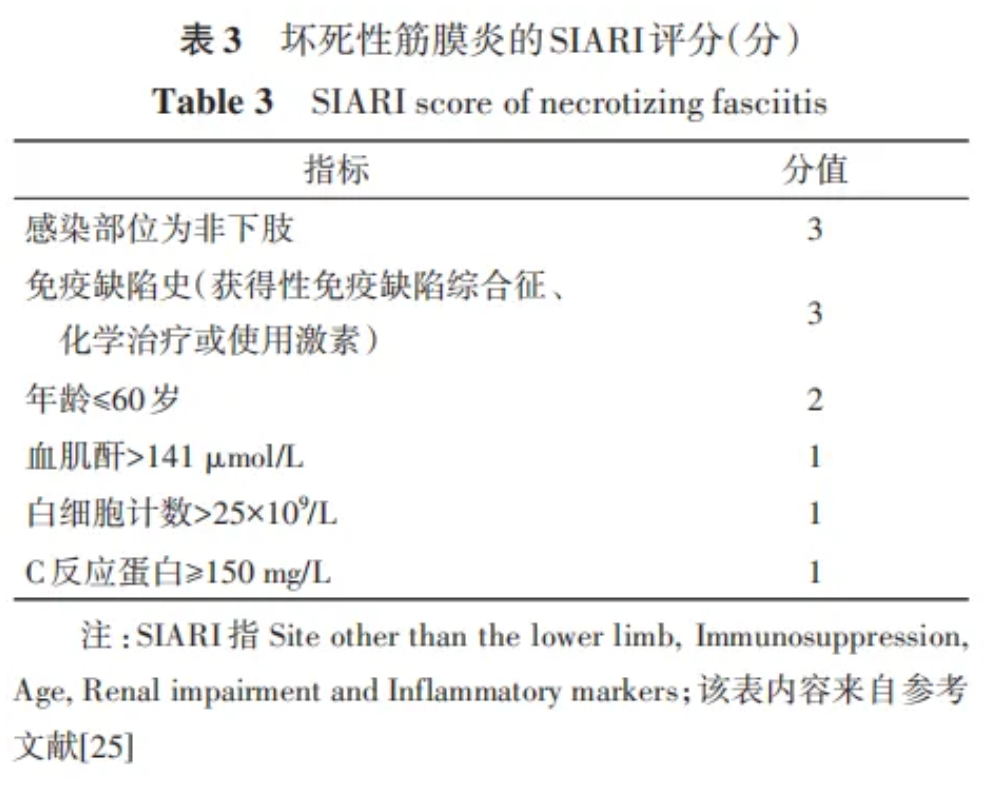
LARINF 评分:以5分作为NF的诊断阈值时,敏感度为84%,特异度为75%,在诊断NF方面具有较高的准确性(表4)。

推荐意见3(强推荐)
针对NF,建议首选CT检查用于急诊筛查,床旁超声用于快速诊断,磁共振成像(magnetic resonance imaging,MRI)用于稳定期辅助鉴别诊断。手术探查及病理检查是NF确诊的金标准,多次微生物培养可用于明确病原体。不推荐单独使用X线检查。证据等级:高。
证据与说明:
影像学检查:
X线检查:与蜂窝织炎相似,NF早期X线主要显示软组织模糊、增厚;部分患者可见筋膜层面气体,此为NF特征之一,但并非普遍存在。不推荐单独用于NF诊断。
CT检查:可清晰显示皮下脂肪变薄、筋膜增厚及小气泡影。凭借其在急诊环境中的适用性,成为辅助NF诊断的首选影像学方法。
超声检查:具有快速便捷的优势,典型表现包括皮下增厚、软组织积气、筋膜积液,部分病例可能出现“鹅卵石样改变”。当超声观察到深度>2mm的液体积聚时,诊断NF的准确性可达72.7%,具有一定的诊断参考意义。
MRI检查:能清晰显示深筋膜增厚、筋膜积液及多隔室受累,尤其在深筋膜积液显像方面优于CT。诊断NF的敏感度高达90%~100%,特异度为50%~85%,是鉴别NF的有效影像学手段。
手术探查及坏死组织病理学检查:
确诊金标准。术中见筋膜肿胀、暗灰、广泛坏死,皮肤及筋膜与肌肉易分离,结合其他检查可高度怀疑;清创时取筋膜做快速活检(染色、培养),观察病理改变可确诊。
微生物培养:
明确病原菌种类及药物敏感情况,可为抗菌药物的合理应用提供依据。这有助于快速控制感染,从而降低患者的截肢率和病死率。
二代测序:
16S核糖体DNA测序较传统培养能更快准确鉴定细菌,为用药提供依据,有望成为早期诊断新手段,仍需进一步研究。
临床问题3:NF的一般治疗
在NF的救治中,早期诊断和及时合理治疗是改善预后的关键。主要包括以下5个方面:早期诊断与彻底清创、广谱抗菌药物治疗、积极的液体复苏、反复病情评估及综合营养支持。
推荐意见4(强推荐)
一旦高度怀疑NF,应尽早进行手术探查,并积极维持呼吸、循环及内环境稳定。证据等级:中。
证据与说明:
术前需尽可能优化患者全身状况,针对不同情况采取对应措施:维持水、电解质平衡,纠正低蛋白血症与贫血;糖尿病患者稳定血糖,脓毒症患者积极液体复苏并按需用药;危重患者可行动静脉置管等支持治疗,同时预防导管相关感染;急性肾损伤患者明确病因后可考虑血液净化;会阴、肛周等特殊部位感染者可予静脉营养支持及灌肠、禁食等处理;凝血功能异常患者针对性补充血液制品,必要时用抗纤溶药物。
临床问题4:NF的抗感染治疗
推荐意见5(强推荐)
在NF的抗感染治疗中,若致病菌尚未明确,应根据流行病学特征及快速革兰染色结果,早期经验性使用足量、规范的广谱抗菌药物,覆盖需氧菌和厌氧菌。随后,根据病原学检测结果及感染标志物的动态变化,调整用药方案。证据等级:高。
证据与说明:
病原体未明确时,全身用抗菌药物可降低细菌载量、抑制毒素生成,是初始治疗重要部分。推荐4种经验性方案:
克林霉素+美罗培南+万古霉素;
哌拉西林/他唑巴坦+万古霉素+克林霉素;
亚胺培南/西司他丁+万古霉素;
头孢曲松+克林霉素+万古霉素。
治疗中需根据培养、基因检测及药敏结果调整为敏感药物,每次手术清创均需采集标本培养指导用药。疗程无统一规范,初始至少48~72小时,严重者可延长至2周。合并脓毒症休克或严重器官功能障碍时,需依据Sepsis 3.0集束化流程,选用高效广谱、起效快的抗菌药物,同时迅速液体复苏及用血管活性药物,维持组织灌注和氧合。
临床问题5:NF的手术治疗
01
推荐意见6(强推荐)
切开清创引流是NF急诊治疗的关键环节。当皮肤出现液波感或明显坏死灶时,应尽早实施手术。术中可使用亚甲蓝标记坏死组织,并多点取样进行病原学检查。首次手术应快速、简单且彻底,重点在于开放潜行腔隙,避免过度清创增加后续修复难度。后续需反复清创,直至彻底清除坏死组织。证据等级:高。
证据与说明:
清创时机:切开清创引流术是治疗NF最为关键的环节。早期外科清创能有效阻止感染的扩散,防止炎症介质释放引发的全身性并发症。入院24h后延迟清创是导致NF患者高病死率死亡相对风险较早期清创增加9倍。在首次清创结束后,若患者病情允许,建议将其转诊至具备多学科联合诊疗条件的三级综合性医院。
清创方法:从明显坏死的皮肤或病灶中心开始切开,向外扩展。直到达健康的软组织并出血;破口小且有潜行腔隙时,注射2~4mL亚甲蓝标记。术中忌用稀释肾上腺素,出血用电凝;用广谱抗菌液冲洗后换生理盐水,引流口小、腔隙大时忌用过氧化氢防气体栓塞。
清创效果:术中多点取样,明确致病菌,选择相对应的敏感抗菌药物和抗菌敷料,创面的边缘组织进行病理学检查确认是否清创彻底,有效清创后,感染指标、局部症状及全身状况均改善,可通过影像学观察创面恢复情况。
推荐意见7(弱推荐)
彻底清创后可使用NPWT促进创面愈合,但明确感染厌氧菌者需慎用,可改用抗菌敷料。证据等级:中。
证据与说明:
NPWT的使用需满足的条件:
创面坏死组织已被彻底清除,感染已得到控制;
创面出血风险低,且患者无严重凝血功能障碍;
厌氧菌感染是NPWT的相对禁忌证,可能导致感染加重。
抗菌敷料:
创面换药是NF治疗的基础手段。
NF术后渗液多,需选择应用吸收性强的敷料,有效管理创面渗液、维持创面湿润平衡,有利于上皮细胞移行,为肉芽组织生长和创面上皮化创造良好条件。
对于坏死组织残留较多的创面,可使用含杀菌功能的敷料进行换药。
若需减轻换药疼痛,可选择亲水纤维敷料或水凝胶敷料等非黏性敷料。
02
推荐意见8(强推荐)
截肢术应谨慎,用于无法控制的致命性肢体感染或功能无法挽救者,手术时机需结合患者全身情况判断。证据等级:中。
证据与说明:
NF患者的截肢率为8.4%,低收入阶层的更高,最常见的截肢部位为手指/脚趾(44.1%)和膝关节以上(22.8%)。截肢的临床预测指标包括糖尿病、软组织肿胀、皮肤坏死、坏疽以及入院时血肌酐≥141 μmol/L。尽早进行抗菌治疗和手术清创,围手术期控制血糖,可降低截肢率。清创后病情无改善且危及生命需二次截肢。出现出血性大疱、合并周围血管疾病、LRINEC评分>8分或菌血症患者,晚期截肢病死率高于早期。新冠大流行期间及之后,NF发病率升高,多与化脓性链球菌感染相关,一半以上患者需截肢或死亡。
03
推荐意见9(强推荐)
治疗 Fournier坏疽时,需评估是否存在肛瘘等肛肠疾病。清创应谨慎,围手术期应严格管理大小便,防止创面污染。证据等级:中。
证据与说明:
Fournier坏疽是一种累及阴囊、会阴、肛周等部位的急性感染性NF。使用钠-葡萄糖共转运蛋白-2抑制剂治疗糖尿病、慢性肾病及心血管疾病时,可能增加 Fournier坏疽的发生风险;男性患者通常无需切除睾丸,仅当影像学显示睾丸积气(提示感染坏死),经评估后可切除,此术可降70%病死率,约21%男性需行患侧睾丸切除术;术前留置尿管及粪便引流袋防污染,尿管插入困难忌强行操作;膀胱造口利于小便管理及后期治疗,结肠造口可减少创面感染、加速愈合。术前需普外科会诊评估粪便转流术,确定造口事宜。大便污染风险高且未行转流术时,建议禁食并予肠外营养。
04
推荐意见10(弱推荐)
创面修复重建是NF治疗的核心,需局部感染得到控制、创面床准备充分、患者全身状况稳定后进行。修复方式可根据创面情况选择,直接缝合、皮片移植、皮瓣移植。对于骨或肌腱暴露的复杂创面及窦道,可选用抗生素骨水泥、富血小板血浆(platelet-richplasma,PRP)或人工真皮支架等材料进行修复。证据等级:中。
证据与说明:
缺损较小且局部组织张力小的可直接缝合;若创基清洁、肉芽组织生长良好,则可直接进行皮片移植;大多数NF患者适合游离皮片移植;非功能部位使用刃厚皮(厚0.20~0.25 mm)移植;功能部位使用 中厚皮(厚 0.35~0.80 mm)移植。复杂创面,可将皮片移植与皮瓣移植相结合,需动态监测移植皮瓣或皮片的血供情况。
抗生素骨水泥:含抗生素,通过缓慢、持续释放抗生素控制感染,减少全身用药。优势:浓度高、作用久、填空腔、安全性高,常用万古霉素等。可形成诱导膜促愈合,Ⅱ期后可植皮,减少手术次数、提高保肢率,无病例死亡。
PRP:含生物活性物质,通过调节炎症反应,促进组织修复与再生。改善血运,促进肉芽组织生长,加速愈合。
人工真皮支架:模拟人体正常皮肤结构和功能。引导细胞迁移和血管新生,直接覆盖暴露的骨和肌腱,防止肌腱粘连,是一种理想的创面床培育方法。
临床问题6:NF的辅助治疗
推荐意见11(强推荐)
有意识障碍、呼吸衰竭或面颈部NF患者,需密切监测局部水肿和呼吸状况。应预防性建立人工气道,阶梯式应用氧疗、辅助通气或机械通气等呼吸支持措施。证据等级:低。
证据与说明:
需重视颈部NF需重视气道管理,该疾病可能导致颈部水肿和组织坏死,增加插管难度。轻、中度呼吸困难者,短期用激素(如地塞米松10mg)及尽早切开引流,通常可避免气管切开;重度呼吸困难且激素无效者,须立即气管切开。合并肺部感染、氧合不佳时,可行阶梯式呼吸支持(氧疗、辅助或机械通气)。需长期气道管理的颈部NF患者,气管切开优于经口/鼻插管,更安全、易固定,且减少并发症。
推荐意见12(强推荐)
不建议使用大剂量糖皮质激素,可考虑静脉注射1g(intravenous immunoglobulin,IVIG)进行免疫支持治疗,但需警惕其可能带来的肾损伤风险。证据等级:中。
证据与说明:
IVIG具有抗炎和免疫调节作用的治疗手段,IVIG 能够中和细菌外毒素和抗原,抑制A组链球菌(Group A Streptococcus,GAS)的毒力因子活性,从而减轻疾病严重程度。IVIG可用于颈部NF患者的强化治疗,对于重度GAS感染的患者,能够降低病死率。但有研究显示其对NF患者病死率和住院时间无显著影响,故建议限于葡萄球菌或链球菌引起的危重坏死性软组织感染。不建议大剂量糖皮质激素,过早使用可能掩盖病情影响诊疗。
推荐意见13(强推荐)
明确病因后,建议采用分级镇痛管理策略。NF是深静脉血栓(deep veinthrombosis,DVT)的高危人群,建议采用分级DVT预防策略。证据等级:低。
证据与说明:
分级镇痛管理策略:NF患者在治疗过程中常经历剧烈疼痛,非特异性疼痛是NF病情变化的重要临床表现,需先排除病情进展再镇痛。明确原因后用非甾体类抗炎镇痛药(如帕瑞昔布);手术范围大、疼痛明显者用多模式镇痛(如冬眠合剂等),需注意该类药物对凝血、胃黏膜及呼吸循环的影响,分级管理参考《急诊创伤疼痛管理专家共识》。
分级DVT管理:NF患者因病程长、卧床久,血流缓慢易形成DVT,入院时应进行宣教、抬高患肢、鼓励患者主被动运动。入院24小时内及每次术后需评估血栓风险,必要时做相关检查,根据结果采取抗凝、溶栓等措施,流程参考《深静脉血栓形成的诊断和治疗指南(第三版)》。
推荐意见14(弱推荐)
对于全身情况相对稳定且可安全转运的NF患者,建议考虑高压氧治疗(hyperbaric oxygen therapy,HBOT)。证据等级:高。
证据与说明:
高压氧治疗能够有效辅助治疗NF,通过增加组织中的含氧量,减少外毒素的释放,抑制厌氧菌的生长,减轻感染,促进新生,加速愈合,对于并发脓毒症休克的NF患者,能够减轻炎症反应,提高生存率。
推荐意见15(强推荐)
建议在治疗过程中早期介入、全程实施个性化综合康复和心理治疗,并将营养支持贯穿整个治疗周期(证据等级:中)
证据与说明:
实施康复和心理治疗:需综合考虑患者的年龄、病变部位、基础疾病、患病前日常生活能力、手术干预阶段及 NF 的严重程度等制订个体化的康复方案。NF治疗周期较长,费用高,患者心理负担加重,长时间处于焦虑状态的应及时开展心理疏导或者心理治疗。
营养支持:较大的创面会导致大量液体和蛋白质流失,NF患者需进行全面的营养评估和营养风险筛查。当营养风险筛查评分>3分时,建议启动营养支持治疗;长时间禁食可能导致营养不良;已行结肠造口,可正常进行肠内营养;未行造口,则建议加强肠外营养,早期营养支持可提高生存率,建议参考相关指南制定流程。
总结与展望
鉴于目前NF治疗相关的临床证据质量低且缺乏针对儿童人群的治疗经验,本共识主要聚焦于成人NF的外科处理策略。总结前期的临床救治经验,为临床医师提供科学、规范的决策参考。
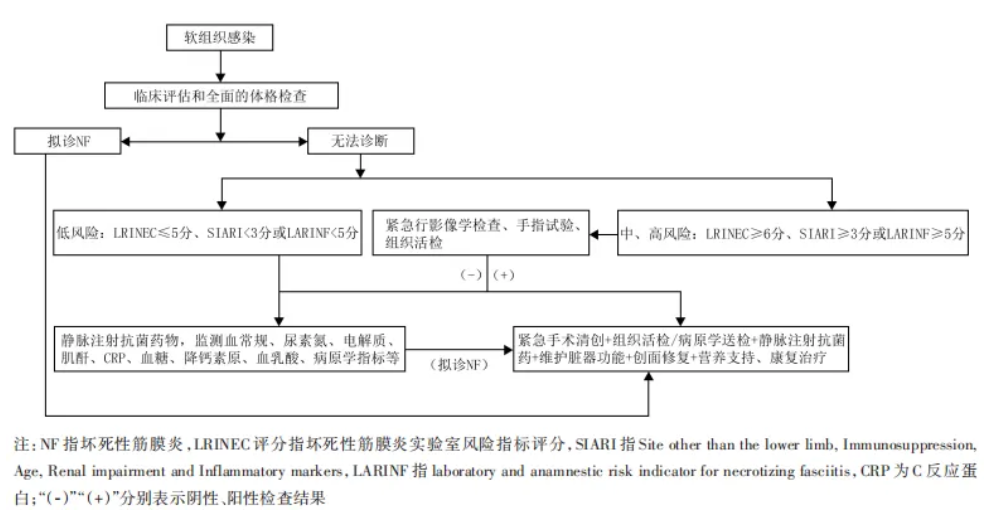
成人NF诊治简化流程图
NF早期诊断难,治疗在疾病认知、诊断技术等方面有局限性。未来可从以下措施提升诊疗水平:提高早期诊断率(用分子诊断技术明确病原体);精准治疗(开发新型抗菌药、优化联合方案);优化手术(推广微创手术);完善辅助治疗(探索生物制剂);加强患者管理(完善康复体系、多学科延续护理);跨学科合作(制定多学科方案);加强技术创新与标准化治疗(用人工智能辅助诊断等)。
参考文献
1.成人坏死性筋膜炎诊治专家共识(2025版),中华医学会烧伤外科学分会 ,《中华烧伤与创面修复杂志》编辑委员会,中国医疗保健国际交流促进会烧伤医学分会
end
全部新闻
100%有效率,百克瑞®系列产品为筋膜组织坏死提供了切实有效的解决方案
全部新闻
【文献分享】成人坏死性筋膜炎诊治专家共识(2025版)
全部新闻
【企业资讯】上海市工商联生物医药商会深入高科生物调研,共探行业发展新路径
全部新闻
9月26-29日!第92届CMEF,上海高科邀您广州见
全部新闻
中国医师节 | 致敬每一位医者
全部新闻
赓续红色血脉 · 同促业务发展
相关阅读
猜您喜欢
- 100%有效率,百克瑞®系列产品为筋膜组织坏死提供了切实有效的解··· 100%有效率,百克瑞®系··· 2025-10-24
- 上海高科生物——中国国际医疗器械博览会的一大亮点 上海高科生物——中国国··· 2024-01-12
- 【邀请函】上海高科邀您参加第22届全国伤口、造口、失禁护理学术··· 【邀请函】上海高科邀您··· 2025-07-07
- 百蒂芬®复合溶葡萄球菌酶 百蒂芬®复合溶葡萄球菌··· 2024-01-14
- 2018年全国肛肠病雄辩争鸣论坛 2018年全国肛肠病雄辩争··· 2024-01-12
- 国家博士后科研工作站 国家博士后科研工作站 2020-12-26
- 2005年 上海市科技进步一等奖 2005年 上海市科技进步··· 2024-01-15
- 乐倍清®口腔护理液 乐倍清®口腔护理液 2024-01-15
 投诉电话:4009203835
投诉电话:4009203835 公司总机:021-55282458
公司总机:021-55282458 HR Email:hr@hi-tech-bio.com
HR Email:hr@hi-tech-bio.com
